Más investigaciones con CRISPR
Ya os hemos hablado muchas veces de esta tecnología (aquí, aquí, aquí y aquí), que ha supuesto una auténtica revolución. Pues bien, cada cierto tiempo tenemos que actualizar un poco, porque cada vez se le encuentran nuevas aplicaciones y maneras de usarla. Vamos ahora a contaros solo algunas, sin ser exhaustivos, porque necesitaríamos mucho espacio para hablaros de todos sus posibles usos.
EDICIÓN DE ÓRGANOS PARA TRASPLANTES
George Church experto en genética de la Universidad de Harvard y cofundador de la empresa eGenesis se embarcó hace unos pocos años en un proyecto para lograr que los órganos procedentes de cerdos fueran compatibles para trasplantarlos a humanos (los trasplantes entre especies se denominan xenotrasplantes). Su idea es emplear la tecnología CRISPR para eliminar los antígenos porcinos frente a los que actúa el sistema inmunitario humano, así como para eliminar virus de los cerdos presentes en estos órganos. Se puso como objetivo 2019 para comenzar la realización de xenotrasplantes de órganos de cerdos modificados con CRISPR. Sin embargo, hoy en día, aún no se ha llegado a ese punto. Actualmente, se están haciendo experimentos de trasplantes de estos órganos de cerdos a monos (babuinos) en el Hospital General de Massachusetts en Boston.

George Church
Uno de los principales problemas para lograr que el xenotrasplante funcione bien radica en que el rechazo a los órganos trasplantados no depende de uno o unos pocos genes, sino de bastantes. Aun así, Luhan Yang, cofundadora de eGenesis, afirma ya están muy cerca de resolver esta cuestión, puesto que han logrado ediciones genéticas de dos dígitos, es decir, han modificado a la vez al menos diez genes diferentes. Podéis ver aquí un charla TED de la doctora Yang sobre los xenotrasplantes:
Por otra parte, diversas organizaciones animalistas, como PETA, se oponen a este tipo de experimentos, no porque sean contrarios a la tecnología en sí, sino a la experimentación con animales. Esto hace que la empresa esté llevando con bastante secretismo todo el proceso.
USAR CRISPR EN EL ESPACIO
Astronautas de la Estación Internacional Espacial han utilizado CRISPR para editar el genoma de una levadura. Estos astronautas estaban trabajando en un proyecto para comprender como funcionan los mecanismos de reparación del ADN en el espacio. La radiación a la que se enfrenta el genoma de cualquier especie en el espacio es mucho mayor que la que recibe en la Tierra y no se sabe si los mecanismos de reparación son los mismos o si son eficaces. El objetivo del experimento era provocar cortes, lesiones específicas en el ADN por medio de CRISPR-Cas9 en la levadura Saccharomyces cerevisiae para mimetizar el daño producido por la radiación. Tras provocar este daño, los astronautas permitieron que la levadura reparara su ADN sin intervenir. Compararon después la estructura molecular del ADN de la levadura antes de que empezara la reparación y después de la misma, para determinar si se había producido algún error genético durante la reparación. Los resultados se publicarán próximamente en un artículo de investigación.
Este experimento fue propuesto por los estudiantes David Li, Aarthi Vijayakumar, Rebecca Li and Michelle Sung como parte del concurso de la NASA Genes in Space.
VACAS QUE PRODUCEN MÁS CARNE
La empresa argentina Kheiron Biotech tiene previsto que para principios del año que viene nazcan los primeros terneros con un genoma editado para que produzcan hasta un 20% más de carne. Además, llegarían a alcanzar el peso ideal en menos tiempo y todo esto consumiendo, según el responsable de la empresa, la misma cantidad de alimento. Para lograr esto se editó el gen de la miostatina para disminuir su expresión. La función de la proteína codificada por este gen es limitar el crecimiento del tejido muscular del animal.

Toro editado genéticamente, de la raza Brangus. Crédito: Gentileza Proinvesa (D. Sempé)
BEBÉS MODIFICADOS GENÉTICAMENTE
Ya hace unos meses saltó la polémica cuando un científico chino anunció que ya se habían logrado los primeros bebés humanos modificados genéticamente. Pues bien, otros científicos de otros países se suman ahora a esta alocada carrera. El científico ruso Denis Rebrikov, del Centro Nacional de Investigación Médica Kulakov ha confirmado en la revista Nature que planea implantar a mujeres embriones modificados genéticamente, para lo cual está ya recabando los permisos y autorizaciones necesarias. Básicamente está trabajando en la edición del gen CCR5, el mismo que editó He Jiankui para lograr una teórica inmunidad frente a la infección por VIH. Rebrikov afirma que su manera de abordar el trabajo es más segura, con mayores beneficios potenciales y éticamente más aceptable que lo que hizo He Jiankui. La principal diferencia es que Jiankui trabajó con embriones de padres con VIH, mientras que Rebrikov lo va a hacer con embriones procedentes de madres con VIH. El riesgo de que un padre infectado con VIH pase el virus a sus hijos es mínimo en comparación con el de que una madre contagie a sus descendientes. Por lo tanto, los posibles beneficios en este caso serían mayores. Además, Rebrikov planea implantar estos embriones en mujeres que no responden al tratamiento con fármacos antiVIH. Pese a todo, el hecho de modificar genéticamente embriones humanos sigue siendo éticamente problemático, como afirma Jennifer Doudna, una de las creadoras de la tecnología.
SIDA
Investigadores de la Facultad de Medicina Lewis Katz de la Universidad de Temple y del Centro Médico de la Universidad de Nebraska han logrado eliminar por primera vez el ADN del VIH-1, responsable del sida, del genoma de ratones. Para ello han utilizado una combinación de la tecnología CRISPR con el uso de antirretrovirales (los fármacos clásicos que se usan para controlar la infección por VIH). Los medicamentos antirretrovirales, utilizados habitualmente en la clínica, actúan impidiendo que el virus se replique, pero no son capaces de eliminarlo del organismo. El ADN del virus permanece “escondido” dentro de las células del enfermo y, cuando se dan las condiciones adecuadas, vuelve a reproducirse. El empleo de CRISPR/Cas9 permite eliminar trozos grandes de este ADN vírico que está latente dentro de las células. Pero por sí solo, tampoco es totalmente efectivo. Ahora, este grupo de investigadores ha asociado el empleo de CRISPR/Cas9 con una nueva estrategia antirretroviral de liberación lenta y acción prolongada, denominada LASER ART. Se trata de un fármaco empaquetado en nanocristales, que se dirigen a los tejidos donde es más probable que el virus se encuentre latente. Estos nanocristales, liberan el fármaco antirretroviral durante semanas, dando tiempo a que CRISPR actúe de manera eficaz, puesto que aumenta el tiempo en el que el virus no se replica.
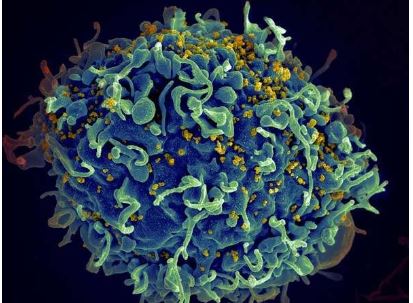
Células infectadas por VIH. Crédito: NIH
MODIFICACIÓN DE VIRUS PARA TRATAR BACTERIAS RESISTENTES
Hace no mucho os contábamos cómo ya se utilizan en terapia un tipo de virus, los fagos, para tratar bacterias resistentes a los antibióticos. Científicos de la empresa Locus Biosciences han desarrollado un cóctel de tres bacteriófagos (abreviadamente llamados fagos) que han sido editados genéticamente con CRISPR, que puede servir como tratamiento para infecciones causadas por bacterias que son multirresistentes a antibióticos. El fago se une específicamente a la bacteria sobre la que se quiere actuar. Dentro de ese fago se ha introducido la herramienta CRISPR, de tal manera que dotan al fago de una ventaja, puesto que cuando el fago inyecta el ADN de CRISPR dentro de la bacteria, la elimina de una manera tremendamente eficaz. En este caso no se ha utilizado la proteína Cas9, la que estamos acostumbrados a asociar a CRISPR, sino otro familiar, Cas3. Y esta diferencia es importante. ¿Por qué? Porque Cas9 hace cortes “limpios” en el ADN de la bacteria, que ésta puede reparar, mientras que Cas3 hace cortes más extensos, casi desgarrando el ADN y es, por lo tanto, más eficaz para matar bacterias. Aquí tenéis un llamativo vídeo de la propia empresa donde explica cómo se hace esto: https://youtu.be/JgXood-oZ1A
A comienzos de 2019 se empezó un ensayo utilizando este cóctel en 20 pacientes en varios hospitales de Estados Unidos, con el fin de determinar, en primer lugar, la seguridad de la terapia. Si los resultados son positivos, se continuará ya con estudios de eficacia en un número mucho mayor de pacientes.
ENSAYO CLÍNICO PARA MIELOMA Y SARCOMA
Ya ha comenzado un ensayo clínico, llevado a cabo por la Universidad de Pennsylvania, en el que dos pacientes con cáncer están siendo tratados por medio de la tecnología CRISPR. Uno de ellos tiene un mieloma múltiple y el otro un sarcoma. En total, en el ensayo participarán 18 pacientes, de sarcoma sinovial, mieloma múltiple, melanoma y liposarcoma. El ensayo no finalizará hasta 2023 y lo que se emplea son célula T editadas genéticamente con la esperanza de que ataquen y eliminen las células cancerosas.
ENSAYOS CLÍNICOS PARA ENFERMEDADES HEMATOLÓGICAS
A finales de 2018 comenzó un ensayo clínico que emplea CRISPR para modificar células madre hematopoyéticas para el tratamiento de la anemia falciforme. En este ensayo participan las empresas Vertex y CRISPR Therapeutics. Recordemos que la anemia falciforme es una enfermedad hereditaria en la que los glóbulos rojos portan una hemoglobina anormal (denominada hemoglobina S). La gravedad varía, según el tipo de anemia falciforme. Hasta ahora, el único tratamiento era el trasplante de médula ósea.







