No es oro solo lo que reluce
El oro, que ha atraído y atrae tanto al ser humano, es el metal precioso por excelencia. Su típico color y brillo se han asociado siempre a riqueza y poder. Es uno de los pocos metales que se encuentran en estado (casi) puro en la naturaleza y resiste la acción del fuego sin ennegrecerse, lo que llamó la atención desde los inicios de la civilización. Sin embargo, aquí te vamos a mostrar cómo las características del oro son mucho más interesantes cuando su color no es el que vemos a diario sino una gama que va del color rojo al morado cuando se encuentra en suspensión y no en estado sólido.
Vayamos paso por paso y empecemos por explicar qué es la nanotecnología. Ésta se puede definir como la síntesis y el estudio de la materia a escala nanométrica, es decir con una dimensión en el rango de 1 nm a 500 nm (aproximadamente). ¿Cómo de pequeño es el nanómetro (nm)?. Un nanómetro son 0.000000001 m, por ejemplo, un pelo mide aproximadamente 100.000 nm de ancho y tus uñas crecen a un ritmo de 1 nm cada segundo. En definitiva, muy muy pequeño, la escala más pequeña antes de entrar en el “mundo” de las moléculas y los átomos. La principal característica de la materia a esta escala es que sus propiedades fisicoquímicas dependen de su tamaño: una partícula que mida 2 nm más que su “compañera” presentará distinto punto de fusión, señal de fluorescencia o color en el visible, como veremos a continuación.
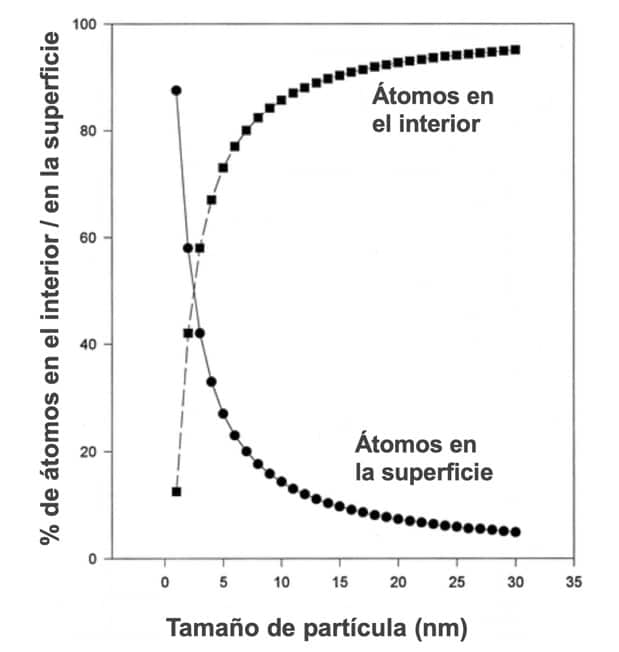
Figura 1. Porcentaje de átomos en el interior y en la superficie en función del tamaño de partícula
Cuando la materia tiene dimensiones nanométricas empiezan a ocurrir fenómenos extraños, al menos si los comparamos con nuestra experiencia diaria en el mundo macroscópico. Una de las características más importantes de la escala nanométrica, es que los átomos que constituyen la materia están, en su inmensa mayoría, en la superficie del objeto (Figura 1). En el mundo macroscópico, en los objetos que nos rodean o en nosotros mismos, el 99.9 % de los átomos están en el interior y el resto en la superficie. En una partícula de tamaño nanométrico (nanopartícula), de unos 3 nm, el 60 % de los átomos están en la superficie. Este hecho cambia completamente sus propiedades fisicoquímicas, haciéndolos, por ejemplo, más reactivos.
Pero volvamos al oro. La química aplicada a la nanotecnología permite producir nanopartículas de oro de forma bastante sencilla y con un buen control de su tamaño. Cuando tenemos nanopartículas de oro dispersas en agua, por ejemplo, alrededor de 5 nm, el color no tiene nada que ver con el que estamos acostumbrados (Figura 2). Con ese tamaño, las nanopartículas de oro presentan un color rojizo similar al del vino tinto, como se puede apreciar en la figura, nada que ver con el típico color del oro a escala macroscópica.
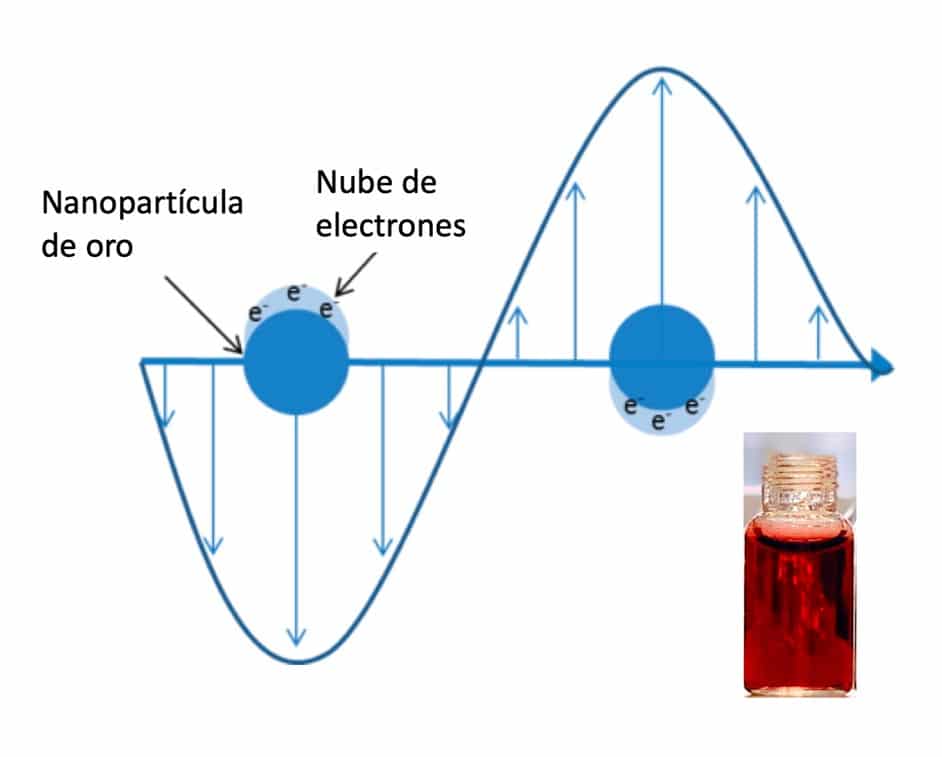
Figura 2. El fenómeno de resonancia del plasmón superficial y nanopartículas de oro en agua.
Pero ¿por qué? ¿Qué ocurre a escala nanométrica para que el color sea tan diferente? Para entenderlo tenemos que explicar el fenómeno conocido como resonancia del plasmón de superficie (SPR en inglés). De forma muy simplificada: cuando tenemos nanopartículas de oro tan pequeñas (también ocurre con otras partículas metálicas), la nube de electrones de los átomos superficiales oscila de forma conjunta al incidir la luz sobre ellos (Figura 2). Esa oscilación se potencia a una determinada longitud de onda (entra en resonancia) produciéndose una gran absorción de luz y apareciendo como color resultante aquél que no se ha absorbido. Por esta razón las nanopartículas de oro, como las de la imagen, presentan un determinado color en función del tamaño (y la forma, pero esa es otra historia). Al incidir la luz visible presentan una banda de absorción muy intensa que produce ese color tan característico.
Este hecho no dejaría de ser algo anecdótico si no fuera por lo que hemos mencionado antes: las propiedades dependientes del tamaño a escala nanométrica. Entonces, ¿qué ocurre si cambiamos el tamaño de nanopartículas de oro como las de la Figura 2? Pues que, al cambiar el tamaño de la nanopartícula, cambiará la longitud de onda de resonancia y, por tanto, el color que observamos de la dispersión de nanopartículas. La Figura 3 muestra nanopartículas de oro de exactamente la misma composición química, pero de diferentes tamaños, lo que hace que el color vaya variando. En este caso, debido a la escala en la que estamos, este fenómeno se produce sin ningún cambio en la composición de las nanopartículas.

Figura 3. Nanopartículas de oro dispersas en agua de tamaños diferentes.
Esta es la clave de la utilidad de estas partículas; ¿qué ocurre si ese cambio de tamaño se produce en función de la presencia o ausencia de una determinada sustancia? Pues que tendríamos un sensor que nos permitirá detectar y cuantificar, de forma rápida y barata, dicha sustancia. Podemos definir un sensor como una sustancia que detecta cambios en su entorno, lo que se traduce en un cambio en una magnitud medible. En este caso, el cambio implica una variación en el tamaño de las nanopartículas, lo que se traduce en un “color” diferente en las nanopartículas.
De hecho, muchas de las personas que estáis leyendo este artículo puede que ya conozcáis este proceso ya que es parte de uno de los sensores in vitro más usados en el día a día: los tests de embarazo. En la figura 4 se muestra de forma esquemática cómo funciona un test de embarazo basado en nanopartículas de oro. Básicamente se trata de un ensayo inmunológico de flujo lateral.
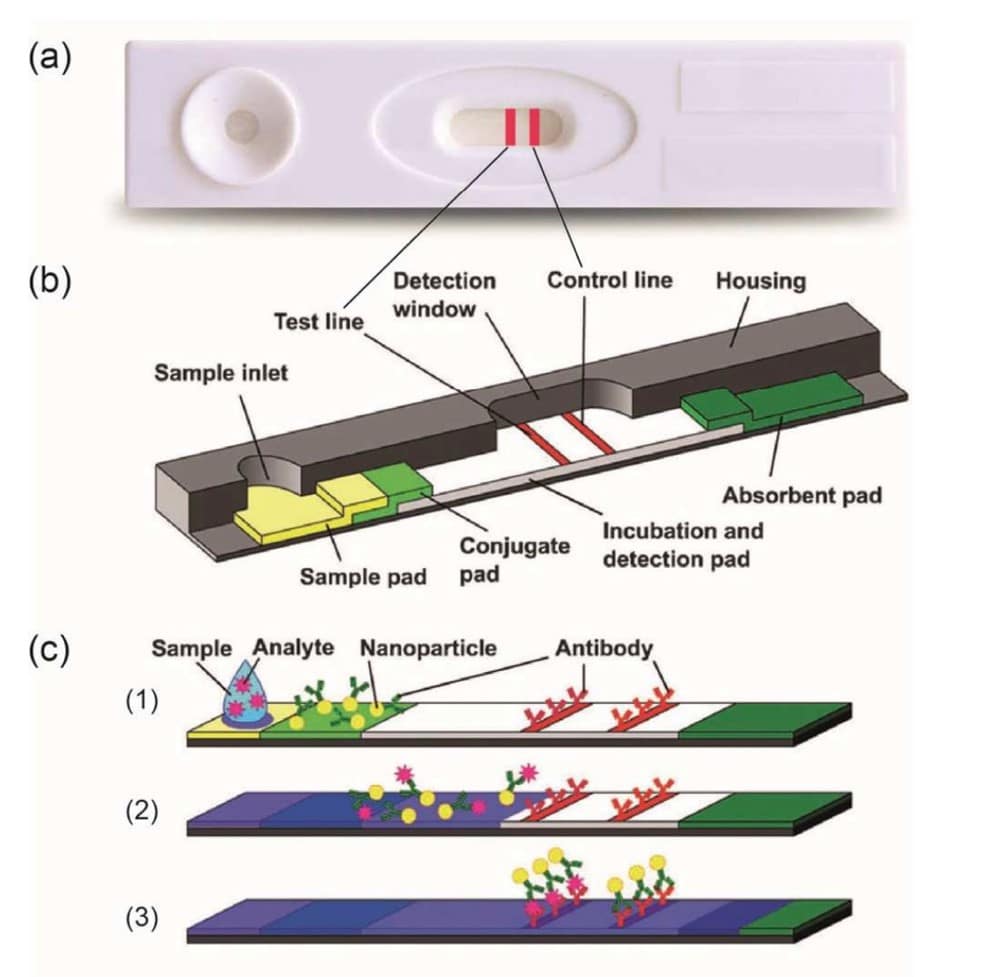
Figura 4. Esquema de un test de embarazo basado en nanopartículas de oro. Reproducido de “Industrial applications of nanoparticles” doi:10.1039/C4CS00362D con permiso de la Royal Society of Chemistry.
Estos dispositivos suelen contar con dos ventanas, una que sirve de control de la medida, indicando que el resultado es válido y otra que nos indica si la medida es positiva o negativa (Figura 4a). Como se observa en la figura 4c (1) hay cuatro zonas diferenciadas. En la primera se deposita la muestra, orina en este caso. En la segunda, se encuentran las nanopartículas de oro, a las que se ha unido químicamente un anticuerpo en su superficie. Dicho anticuerpo reconoce el analito (sustancia presente en la orina que queremos detectar o cuantificar) , que en este caso se suele tratar de la hormona gonadotropina coriónica humana (HCG, human chorionic gonadotropin), la cual se produce en la placenta durante el embarazo. En la tercera se encuentra un anticuerpo que también reconoce el analito y, la última, consiste en la línea control, que lleva un segundo anticuerpo que reconoce el primer anticuerpo unido a las nanopartículas para comprobar la validez de la medida. Al depositar la muestra, el líquido arrastra las nanopartículas, al llegar a la banda de detección, si el analito está presente, las nanopartículas se unirán mediante su anticuerpo y tendremos un positivo, a continuación, si la medida ha sido correcta se unirán a la segunda línea de anticuerpos para validar la medida (Figura 4c (3)). Además, debido a las excelentes propiedades ópticas de las nanopartículas, la cantidad que hay que usar para generar una banda coloreada que sea claramente visible es mínima.
Este es solo un ejemplo de cómo las propiedades dependientes de tamaño, que caracterizan a los nanomateriales, se pueden emplear para el diagnóstico in vitro, como en el caso del test de embarazo, o in vivo en ejemplos de imagen médica.
Para saber más:
(1) Stark, W. J.; Stoessel, P. R.; Wohlleben, W.; Hafner, A. Industrial Applications of Nanoparticles. Chem. Soc. Rev. 2015, 44, 5793–5805.
(2) https://www.quo.es/salud/a25405289/pruebas-para-detecta-el-cancer/
(3) Chang, C.-C.; Chen, C.-P.; Wu, T.-H.; Yang, C.-H.; Lin, C.-W.; Chen, C.-Y. Gold Nanoparticle-Based Colorimetric Strategies for Chemical and Biological Sensing Applications. Nanomater. (Basel, Switzerland) 2019, 9.
About the Author: Fernando Herranz
2 Comments
Leave A Comment Cancelar la respuesta
Este sitio usa Akismet para reducir el spam. Aprende cómo se procesan los datos de tus comentarios.








[…] unos 4 años. La segunda noticia es un artículo que Fernando Arranz publica en DCiencia sobre las propiedades del oro en solución. ¿Sabrían decirme, antes de leerlo, de qué color es el oro? Se sorprenderán de las […]
[…] hace unos 4 años. La segunda noticia es un artículo que Fernando Arranz publica en DCiencia sobre las propiedades del oro en solución. ¿Sabrían decirme, antes de leerlo, de qué color es el oro? Se sorprenderán de las […]