Los mecanismos moleculares del éxito de la infectividad en la covid-19: ¿Un problema para la eficacia de las vacunas?
Por Víctor Ladero y Emilio Muñoz, de la Asociación Española para el Avance de la Ciencia.
Introducción
Antes de entrar en profundidad en los mecanismos moleculares que han hecho del SARS-CoV-2 un virus muy eficiente, y que con una meditada estrategia operativa se ha extendido por todos los países, haciendo que la enfermedad que provoca, covid-19, haya sido declarada pandemia mundial por la Organización Mundial de la Salud (OMS) [1], queremos saludar al periodismo científico de calidad. Para quienes somos devotos seguidores de la divulgación científica y esforzados cultivadores de la misma es motivo de satisfacción la publicación el domingo 10 de mayo de 2020 de un artículo que marca un hito en la relativamente joven historia de la comunicación científica en nuestro país [2].
Manuel Ansede, A. Galocha y M. Zafra han publicado un texto de primer nivel, tanto en el estilo como en la forma, con un magnifico esfuerzo en la consulta de fuentes y un derroche infográfico que se sitúa en la línea de los textos que publica desde sus orígenes la revista líder Scientific American (y su versión española Investigación y Ciencia) con otro dato significativo: se acerca a una línea editorial que la puntera revista empezó hace unos pocos años y que consiste en que los relatos de los temas científicos de actualidad y éxito no se contribuyeran solo por destacados científicos sino de modo progresivo por lo que llaman escritores sobe ciencia “science writers”.
En estos apasionantes tiempos de la investigación científica sobre la Covid-19, el texto que glosamos empieza por atraer la atención con el título, ”La secuencia de 12 letras que ha cambiado el mundo” y el siguiente antetítulo: “Los científicos creen haber encontrado la virulencia del patógeno” [2]. Otra contribución notable de este trabajo periodístico para los que somos defensores de la interdisciplinariedad es que los autores han optado por esa visión en la selección de las fuentes, otra sorpresa en el ámbito de la comunicación de la ciencia en España.
El proceso de la infección
Lo que el texto describe es cómo se produce el mecanismo de infección de un virus dotado de una estructura muy especial. Su imagen está haciendo fortuna pues preside todos los programas televisivos sobre la crisis y ha habido hasta diseño de joyas -el poder del morbo. El SARS-CoV-2 tiene apariencia de monstruo que genera miedo [3].

Estructura del virus SARS-CoV-2. Fuente: modificada de rebelem.com
Esta llamativa estructura encierra el ARN, la molécula que es la responsable de almacenar la información que ha contribuido a su “éxito”, protegida por un núcleo proteico (nucleoproteína) y a su vez rodeada por una membrana lipídica (envoltura) que se ven coronadas por las espículas (proteína S), glucoproteínas, que son la llave para la entrada en las células del huésped a través de la puerta (ACE2) [4]. Una vez en el interior de las células, estas van a ser engañadas para que el ARN viral, el código genético que va a predominar para multiplicarse, se copie a sí mismo, y pasa a controlar la célula infectada y a dar las órdenes para crear miles de nuevas partículas víricas que se extenderán, de forma silenciosa, por el organismo y de éste a otros que estén en contacto o en la cercanía, comportándose como un parásito, un reproductor subrepticio.
La actuación de la espícula
En el artículo, la primera y más importante fuente en términos de relato, tiene que ver con un científico, Gregory R. Bowman, que trabaja en la estructura de proteínas -de nuevo una sorpresa en la comunicación científica española- tema sobre el que podemos apostar que ha ocupado apenas el 1 por ciento desde que la comunicación sobre ciencia existe en nuestro país. Gregory R. Bowman [5], es profesor de Química en la Facultad de Medicina de la Universidad Washington de St. Louis, Missouri. Lidera un programa de supercomputación relacionado con la estructura de proteínas, FoldingHome (Plegamiento en casa) (https://foldingathome.org/start-folding/). A diferencia de lo que ocurre en España donde existe un Centro Nacional de Supercomputación en Barcelona (https://www.bsc.es/es), dotado de unos pocos ordenadores de alta capacidad de cálculo, Bowman, siguiendo el modelo que se inició en Stanford hace años, recurre al poder de computación casero de cientos de miles de seguidores: es lo que en sociología y política de la ciencia se ha llamado con mayor o menor fortuna “ciencia participativa”. Bowman es un científico bastante excepcional, tiene una discapacidad visual reconocida (ceguera legal) a causa de una enfermedad macular degenerativa que hizo crisis sobre los nueve años. Le apasionaba la biología y la investigación, aunque sabía que no podía funcionar en el mundo de la pipeta y los análisis espectrométricos, lo que le llevó a optar por la vía que fundó su director de tesis Vijay Pande en la Universidad Stanford como ya se ha mencionado anteriormente.
Ahora, con motivo de la emergencia sanitaria generada por la Covid-19 está trabajando con su grupo, que destaca en los estudios sobre dinámicas de las proteínas, en el proceso de entrada del virus en las células donde va encontrar el receptor, que está altamente distribuido por diferentes órganos [4].

Proceso de inicio de la infección por SARS-CoV-2, la proteína de superficie S, la espícula, reconoce el receptor celular (ACE-2), cambia su morfología y se une a él. Para ello, se abre, cual Demogorgon y parece engullir al receptor. Fuente: elaboración propia; imagen tomada de Fortnite-wiki.
Bowman, explora la relación de la cerradura con esa llave con apariencia de cabeza monstruosa a la que en su laboratorio llaman “el Demogorgon, el monstruo de Stranger Things [6], como señala el artículo de Ansede y colaboradores. La analogía parece perfecta puesto que la estructura de trímero (tres subunidades) de la espícula recuerda a una planta carnívora. La afinidad con la que la espícula del SARS-CoV-2 se une al ACE2 es superior en un orden de magnitud (entre 10 y 20 veces) a la del SARS de 2002. Sin embargo, cuando queremos entrar a través de una puerta cerrada, no es suficiente con que nuestra llave encaje en la cerradura, debemos además girarla para de esta forma abrirla permitiéndonos la entrada. De igual forma, cuando un coronavirus une su espícula al receptor es necesario que se produzca una activación, mediada por proteasas celulares, antes de fusionar su membrana y así introducir su ARN en la célula a infectar.
Esta activación, en el caso de SARS-CoV-2, está mediada por proteasas como la TMPRSS2 (siglas del inglés para la serinproteasa transmembranal) y las catepsinas, que cortan la espícula y facilitan el proceso de fusión de la membrana vírica con la de la célula a infectar. Pero lo que hace al agente infeccioso de la covid-19 más eficiente es una peculiaridad novedosa en este proceso, ya que la espícula “tiene un punto de corte adicional” que la convierte en sustrato para una tercera proteasa, la furina. Este sitio de corte adicional está codificado por una inserción de doce nucleótidos, las doce letras extra de su ARN, que cuando son leídas añaden cuatro aminoácidos que son reconocidos por esta proteasa.

Secuencia de los doce nucleótidos presentes en el ARN del SARS-CoV-2 responsables de la aparición de un sitio de corte para la furina en su espícula.
El papel de la furina en la dispersión del SARS-CoV-2
La furina es una proteasa, de la cual se puede encontrar una amplísima descripción en la Wikipedia [7], de distribución ubicua entre las células humanas. La furina, está codificada por el gen FURIN, concretamente por la región superior del gen conocido como FES (FES Upstream Region) y de aquí le viene el nombre. La furina forma parte de la familia de las convertasas pre-proteina (actúan sobre proteínas que necesitan un corte para ser activas) del tipo de la subtilisina.
En la entrada en Wikipedia sobre furin(a) se presenta la enorme cantidad de procesos y sustratos sobre los que interviene esta proteasa. Las doce letras que constituyen la secuencia diferencial corresponden a dos aminoácidos básicos que forman parte de zona de corte con la siguiente secuencia ArgX-(Arg/Lys) –Arg, en la porción N-terminal de la proteína. Aunque lo más significativo para entender el papel que juega en la dispersión de este coronavirus es su gran abundancia en el aparato de Golgi, el orgánulo celular encargado de conducir a las proteínas sintetizadas en el retículo sarcoplásmico para exportarlas, tras su modificación, al resto del organismo formando vesículas. La furina actúa sobre un alto número de proteínas, de las que podemos destacar las integrantes de las envolturas de otros virus: gripe, dengue, ébola, y marburg.
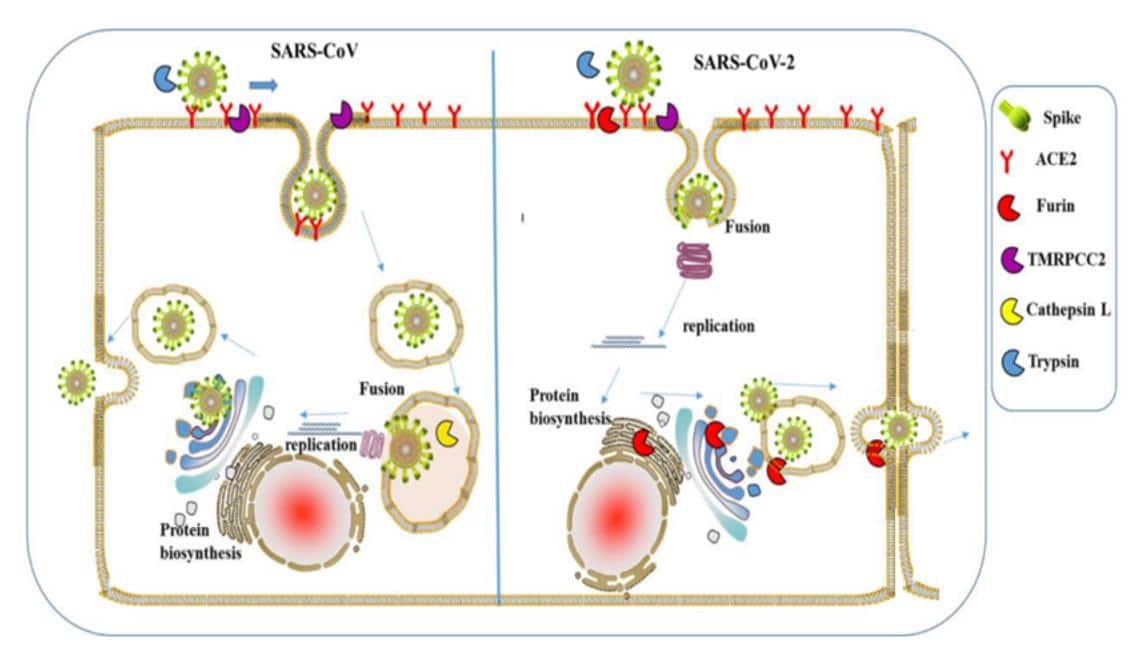
Diferencias entre el modo de dispersión entre SARS-CoV y SARS-CoV-2, tras la acción de la furina las nuevas partículas virales pueden entrar en una célula adyacente sin necesidad de salir al torrente sanguíneo. Fuente: http://chinaxiv.org/abs/202002.00062.
Tras la fusión del coronavirus con la célula infectada, se produce la entrada del ARN viral y se activa la maquinaria de multiplicación del virus, gracias a la apropiación del código genético de la célula, y la producción de partículas virales. Cuando éstas están en el aparato de Golgi, sufren la acción de la furina lo que consigue que las partículas virales se preactiven dentro de la célula, facilitando la fusión de su envoltura con otra célula adyacente, sin necesidad de transporte alguno al exterior celular, creando así un mecanismo parecido a la endocitosis, con lo que los virus pueden circular protegidos sin entrar en el torrente sanguíneo y mostrando un comportamiento que recuerda al del virus del sida.
Implicaciones para el desarrollo de una vacuna
Este comportamiento de protección celular, unido a los fracasos continuos en la obtención de vacunas frente al sida, suscitan dudas, no solo a quienes esto escriben sino a personalidades e instituciones más importantes; como las expresadas en el senado de los Estados Unidos y ante la OMS por el Dr. Anthony Fauci. De igual forma, nuestro colega y amigo el Profesor Vicente Larraga, investigador del CSIC que trabaja en el desarrollo de una vacuna frente al coronavirus [8], y que posee experiencia previa en la obtención de vacunas contra parásitos, que no viajan por el torrente sanguíneo ya que están dentro de las células, sostiene la necesidad de tener, no una, sino varias vacunas diferentes, para tratar de superar esta dificultad añadida creada por el peculiar modo de transmisión del coronavirus en nuestro organismo, y que estas vacunas sean capaces de, además de generar anticuerpos neutralizantes, inducir inmunidad celular.
Afortunadamente, hay muchos grupos trabajando en el desarrollo de una vacuna frente al coronavirus, con diferentes estrategias [9], incluidas las que se están desarrollando en España [10]. Algunas de estas vacunas ya se han empezado a realizar ensayos en humanos [11], la denominada fase II de los ensayos clínicos necesarios para comercializar y administrar una vacuna segura y eficaz, estando a la cabeza de estas investigaciones vacunas desarrolladas en China, Estados Unidos y Gran Bretaña. De algunas de ellas, se van conociendo los primeros resultados de los que se puede deducir que ninguna de ellas parece haber generado anticuerpos en todos organismos en los que se ha ensayado [12].
Otro problema, al que como sociedad deberemos enfrentarnos, será la disponibilidad de estas vacunas una vez estén listas. Ninguna empresa tiene la capacidad de producir 16.000 millones de dosis; la demanda global necesaria, y menos aun manteniendo la producción de vacunas frente a otras enfermedades que siguen siendo necesarias. Solo en España, serían necesarias unos 100 millones de dosis, para poder vacunarnos a todos [13], como sostiene el virólogo Florian Krammer, del Hospital Monte Sinaí de Nueva York. Por ello, el hecho de que estén en curso varios tipos de vacunas, con diferentes estrategias, se hace aún más necesario, pensando en la posibilidad de que varias de ellas sean lo suficientemente efectivas para que se puedan administrar al ser fabricadas en diferentes partes del mundo. Tanto la OMS, como iniciativas privadas como la de la Fundación Bill y Melinda Gates, están desarrollando plataformas que pretenden contribuir al desarrollo de la vacuna, pero también garantizar una producción y una distribución justas, tratando de no dejar atrás a los países con menos recursos [14], aunque muchos países ya está cerrando acuerdos que garanticen el acceso prioritario a sus ciudadanos.
Corolario; apuntes sobre el futuro
En el constante debate entre los egoísmos, los intereses y la ética de la responsabilidad, debemos apoyar esta última y aplicar desde la ciencia y su metodología. Es lo que, en estos tiempos de pandemia, diversos artículos han planteado como un conflicto entre la bolsa y la vida [15].
Para ello se hace necesario un movimiento regeneracionista que se apoye en un consecuencialismo basado en valores. Por mucho que sea sensible, hay que asumir el riesgo de lo que declaramos a continuación: ya no vale la ética “de los grandes principios”, solo desde la filosofía moral, pues estas aproximaciones se quedan alicortas por falta de visión acerca de las dimensiones multi e interdisciplinares que caracterizan las complejas circunstancias actuales. El concepto de INTERÉTICAS se ha propuesto y utilizado para analizar y aplicar en cuestiones complejas [16]. Sobre estos activos debemos apostar por un pacto mundial apoyado en el multilateralismo con la connivencia de todos los banqueros y agente económicos que quieran caminar por una vía que tenga como mojones la SOLIDARIDAD y la SOSTENIBILIDAD. La empatía con la sociedad y con la naturaleza es el futuro, futuro de unas democracia y ciencia asociadas y responsables [17].
REFERENCIAS
[2] https://elpais.com/elpais/2020/05/09/ciencia/1589059080_203445.html
[3] https://aeac.science/covid19-miedo-e-incertidumbre/
[5] https://foldingathome.org/author/gbowman/
[6] https://www.netflix.com/es/title/80057281
[7] https://en.wikipedia.org/wiki/Furin
[11] https://www.the-scientist.com/news-opinion/covid-19-vaccine-frontrunners-67382
[13] https://elpais.com/ciencia/2020-05-21/china-sera-la-primera-en-tener-la-vacuna.html
[14] https://www.elconfidencial.com/tecnologia/2020-05-08/vacunas-coronavirus-covid19-sarscov2_2584908/
[15] https://theconversation.com/covid-19-el-dilema-diabolico-entre-salvar-la-bolsa-o-la-vida-136917
[16] https://aeac.science/re-evoluciones/
[17] https://theconversation.com/en-que-se-parecen-ciencia-y-democracia-120326
Autores
Este artículo ha sido elaborado por:
Emilio Muñoz, socio promotor de la AEAC, nace en Valencia en 1937. Es Doctor en Farmacia, Profesor de Investigación del Consejo Superior de Investigaciones Científicas en el área de Biología y Biomedicina. Actualmente vinculado “ad honorem”en el Instituto de Filosofía del CSIC, Departamento de Ciencia, Tecnología y Sociedad.
Víctor Ladero, Científico Titular en el Grupo de Microbiología Molecular de Instituto de Productos Lácteos de Asturias (IPLA-CSIC) y socio fundacional de la Asociación Española para el Avance de la Ciencia (AEAC).
About the Author: Victor Ladero
7 Comments
Leave A Comment Cancelar la respuesta
Este sitio usa Akismet para reducir el spam. Aprende cómo se procesan los datos de tus comentarios.







Gracias como siempre por tus artículos, y tu pasión. Sin embargo, no tengo nada claro de una nueva etica o interética con la cual salvar contradicciones, es más, me parece pura retórica. No eres el único, en la misma línea va el artículo de M. Morse and J. Loscalzo | DOI: 10.1056/NEJMp2002502 | June 10, 2020 NEJM por una justicia social y racial en salud a traves de formación en la misma. Una cosa es saber si tal o cual medicamento funciona bien en tal o cual comunidad y otra cosa aprenderte el número de autobus de Rosa Park para el examen de de Anatomía Patológica. Pienso que el racismo no se combate con la creación de estudios de raza, ni la pobreza con observatorios sobre la pobreza. Ese enfoque es un error de dimensiones tan enormes que si no se ve es porque no lo abarca la mirada. Los mojones sólo te indican el Km y la carretera, no la cantidad de baches ni de curvas que tiene. Introducir a los bancos en el debate sólo me recuerda lo mucho que cuesta la investigación en biología molecular y el coste desorbitado de la terapia celular. ¿Es entonces ética este tipo de investigación? Parecemos respetar una educación para esos valores pero quizás debería plantearse más si nuestra práctica los respeta. Ese corolario me ha dejado muy preocupado.
Muchas gracias por el comentario y el interés que demuestra.
Quizá uno de los elementos más positivos del mismo es la declaración de que el corolario le haya dejado preocupado. Ese era precisamente su objetivo: pasar de lo descriptivo a lo propositivo y con ello introducir elementos para la reflexión, la duda, avanzar vías para soluciones. Parece que desde hace tiempo se reconoce que estamos en sociedades, o en un mundo, plagadas de incertidumbres, de imprecisiones en muchas facetas profesionales, y de contradicciones a todos los niveles.
El concepto de interéticas que acuñó uno de nosotros para dar trayectoria, abrir un camino, a las dimensiones y dinámicas éticas de la investigación en tecnologías tan complejas como las biotecnologías y en enseñanzas arriesgadas como la ética en las ingenierías, parece interesante que se lance a la palestra, que se proponga ante las características sociales antedichas, y mucho más en esta situación de la pandemia covid-19. Se hace difícil gestionar este universo desde una sola disciplina por importante que se considere como es la economía. En la gestión y sufrimiento de la pandemia están implicados todos los agentes del siglo XXI. Cada agencia tendrá, deberá tener, sus códigos éticos (lo que se llamaba deontologías). Por comentar un ejemplo del valioso comentario: no se propone que el racismo se combata con estudios sobre raza-concepto discutido en biología- sino con la intervención de profesionales con diferentes formaciones, visiones y perspectivas desde la filosofía a la arquitectura y las ingenierías.
Y, si como se pregunta, la práctica no respeta los valores, habrá que cuestionar, y muy seriamente, las prácticas.
Emilio Muñoz
Victor Ladero
[…] https://www.dciencia.es/los-mecanismos-moleculares-del-exito-de-la-infectividad-en-la-covid-19-un-pr… […]
[…] Este virus está poco a poco revelando sus secretos a los científicos: conocimos su secuencia, lo que permitió el diseño de test de detección y de vacunas, y también algunas particularidades, como un sitio de corte para la proteasa furina que le ayudaría a pasar de una célula a otra escapando de la acción de los anticuerpos. […]
[…] de detección y de vacunas, y también algunas particularidades, como un sitio de corte para la proteasa furina que le ayudaría a pasar de una célula a otra escapando de la acción de los […]
[…] de detección y de vacunas, y también algunas particularidades, como un sitio de corte para la proteasa furina que le ayudaría a pasar de una célula a otra escapando de la acción de los […]
[…] https://www.dciencia.es/los-mecanismos-moleculares-del-exito-de-la-infectividad-en-la-covid-19-un-pr… […]