Estrategias para frenar el envejecimiento
Hace no mucho publicamos en Dciencia un post en el que os explicábamos las características del envejecimiento. Hoy vamos a hacer una especie de segunda parte sobre un tema que seguramente os interese aún más: ¿cómo frenar el envejecimiento?
Hoy en día las terapias antienvejecimiento están muy de moda. Podemos leer o escuchar en multitud de sitios muchas ideas y acciones para retrasar ese fenómeno inexorable que es el envejecimiento. No hace falta decir que mucho de lo que se escucha son simplemente actividades de marketing o pseudociencia. Aquí vamos a abordarlo desde un punto de vista exclusivamente científico. Os vamos a contar lo que realmente se sabe y lo que se está estudiando. Nada más.
¿CUÁL ES EL OBJETIVO DE LOS LABORATORIOS QUE INVESTIGAN EL ENVEJECIMIENTO?
La idea principal es identificar dianas farmacológicas (es decir, moléculas, vías, procesos celulares sobre los que se puede intervenir) que puedan mejorar la salud de las personas durante el proceso del envejecimiento. Como ya dijimos en el anterior post, el objetivo no es, ni debe ser, la inmortalidad. Se puede retrasar el envejecimiento, alargar el período de vida, pero de lo que se trata es de mejorar la salud para que muchos lleguemos a una edad avanzada viviendo bien, con buena calidad.
En el laboratorio se ha logrado aumentar los años de vida saludables en varias especies animales, utilizando intervenciones diversas. Sin embargo, tenemos que recordar que esto no es inmediatamente trasladable a humanos, así que siempre hay que ser muy cauteloso.
Vamos a comentar ahora algunas de las estrategias que se han estudiado para frenar el envejecimiento o lograr que sea saludable.
ANTIOXIDANTES
Una de las causas que se relacionan con el envejecimiento es el estrés oxidativo. Sabemos que el oxígeno es indispensable para la vida. Sin embargo, cuando el oxígeno participa en procesos intracelulares, en determinadas reacciones químicas (por ejemplo, la utilización de azúcares y grasa para la obtención de energía) se produce lo que se denominan radicales libres de oxígeno. Estos radicales libres son agentes oxidantes. En nuestro organismo hay mecanismos antioxidantes para compensar la presencia excesiva de estos radicales libres. Entre ellos, todos conocemos las vitaminas A, C, E o la coenzima Q10.
Si se piensa que el envejecimiento puede estar relacionado con la oxidación, es bastante inmediato pensar que si tomamos antioxidantes se podría retrasar el mismo. Sin embargo, los estudios no son concluyentes. Así, podemos encontrar trabajos en los que se observa que el incremento global de las defensas antioxidantes del organismo podría retrasar el envejecimiento y las enfermedades asociadas a la edad en ratones. Sin embargo, es difícil encontrar estudios en personas en los que se encuentre una correlación clara entre la suplementación de la dieta con antioxidantes y un efecto positivo en la longevidad o el envejecimiento saludable.
RESTRICCIÓN CALÓRICA
Es una intervención de carácter metabólico que consiste en reducir la ingesta de calorías sin provocar, obviamente, malnutrición. Se trata de la única intervención que puede prolongar la longevidad en todas las especies en las que se ha estudiado hasta el momento, desde levaduras hasta primates.
Sin saber mucho de biología molecular, pensar que la restricción calórica puede ayudarnos a frenar el envejecimiento y prolongar la vida parece bastante obvio. Si recordamos el post “Cambios biológicos en el envejecimiento”, uno de los puntos característicos de este es la mala función mitocondrial, que provocaba la aparición de radicales libres de oxígeno que, como hemos comentado anteriormente, provocaban oxidación en nuestras moléculas y daños en las mismas. Nuestro organismo, simplificando mucho, utiliza la comida para obtener materiales y energía. La obtención de esta energía se hace, fundamentalmente, en las mitocondrias. Todo esto se realiza mediante reacciones químicas que requieren la participación de oxígeno y en las que se generan estos radicales de oxígeno que son nocivos. Lógicamente, si reducimos la ingesta, reducimos la producción de radicales libres y por tanto la oxidación, causando menos “daño” a nuestras células.
Pues bien, efectivamente se ha comprobado que al restringir la cantidad de alimento entre un 10 y un 40% se consigue alargar en unas tres veces la vida de las levaduras o en un 40% la de los ratones (ver imagen). Otros experimentos han logrado prolongar la vida de los monos Rhesus entre 7 y 14 años.
Efecto de la restricción calórica y de determinadas mutaciones o uso de fármacos en la esperanza de vida y efectos sobre la salud

Imagen tomada de Fontana L et al Dietary Restriction, Growth Factors and Aging: from yeast to humans, Science (2010)
Pero, como podéis ver en la imagen, y seguro que os esperabais, en los seres humanos no está tan claro. Así, hay estudios en los que se observa que la restricción calórica sí mejora la esperanza de vida de personas que sufren de obesidad o sobrepeso. En cualquier caso, sí que se observa un conjunto muy importante de efectos beneficiosos en la salud. Por lo tanto, aunque no esté todavía totalmente demostrado que la restricción calórica alarga la vida en humanos, sí podemos afirmar que lo que sí hace es que los años que vivamos sean más saludables.
Podemos pensar que practicar una reducción de las calorías que ingerimos de entre un 20 y un 40% es complicado. Pues bien, parece bastante establecido que una estrategia alternativa, el ayuno intermitente, es igualmente efectiva. El ayuno intermitente no consiste en no comer durante una semana y luego otra sí. Se trata de ayunos de horas o, como mucho, días alternos, si bien aún no se ha establecido una pauta óptima. Así, se ha demostrado que restringir el acceso a la comida durante unas pocas horas al día es suficiente para mejorar la salud y longevidad en ratones, incluso cuando se compara con ratones que tenían acceso libre a comida pero que ingerían el mismo número de calorías que los que tenían las horas restringidas.
¿Cómo logra estas mejoras la restricción calórica? A través de varios mecanismos. Por una parte, provoca una reducción en el peso, lo cual alivia las complicaciones físicas de la obesidad, como la sobrecarga articular. Aparte de estos aspectos mecánicos, la restricción calórica elimina tejido adiposo, sobre todo la grasa visceral, que es particularmente nociva para un envejecimiento saludable, debido a su capacidad proinflamatoria y diabetogénica. También mejora la función inmunológica.
Individuo antes de practicar la restricción calórica a la izquierda y tras siete años de restricción (derecha). Sus niveles de presión arterial bajaron de 144/87 mm Hg a 94/61 mm Hg. Su colesterol total de 244 mg/dl a 165 mg/dl

Imagen tomada de Fontana L et al Dietary Restriction, Growth Factors and Aging: from yeast to humans, Science (2010)
COMPUESTOS QUE MIMETIZAN LA RESTRICCIÓN CALÓRICA
Con esto nos referimos a agentes, moléculas, que provocan cambios en el organismo que son similares a lo que sucede cuando existe una restricción calórica. Existen numerosos compuestos de este tipo, pero sin duda uno de los más conocidos es el resveratrol. Se ha visto que es capaz de prolongar la vida en nematodos y tanto la vida como el tiempo de vida saludable en ratones obesos., efecto que se ve acompañado por una disminución en la inflamación, mejora en la coordinación motora, mejora en la sensibilidad a la insulina…
RESTRICCIÓN PROTÉICA Y AMINOACÍDICA
Hay varios estudios sobre la relación entre macronutrientes y la esperanza de vida en ratones que han confirmado la relación entre la salud y la longevidad con una sustitución de proteínas por carbohidratos.
Por otra parte, también hay estudios que determinan que una dieta en la que se elimina específicamente el aminoácido metionina puede extender la longevidad en varios modelos animales, desde levaduras hasta roedores. Esto se debe a varios mecanismos moleculares demasiado complejos como para explicarlos aquí. Baste decir que tiene relación, entre otras cosas, con los procesos epigenéticos que ya vimos que eran importantes en el envejecimiento.
Se han empleado en ratones dietas con pocas calorías y proteínas, que se administran sin restricción pero que imitan a regímenes de ayuno. Estas dietas, administradas a ratones de mediana edad en pautas de, por ejemplo, cuatro días al mes, han logrado disminuir la grasa visceral, la incidencia del cáncer, rejuvenecer el sistema inmune y extender la longevidad. Se han probado también en pacientes en pautas similares (se trata de dietas con el 45% más o menos de la ingesta calórica media y con 10% de proteínas) y se han observado efectos moleculares interesantes, que parece que también van en la línea de lo que sucede con los ratones.
METFORMINA
Cualquier diabético conoce esta molécula. Es un antidiabético oral. Es decir, es un fármaco que tras ingerirse y absorberse disminuye la glucosa en sangre. Curiosamente parece ser que parte de sus efectos beneficiosos no los realiza directamente sobre alguna molécula de nuestro organismo, sino por medio de cambios en la microbiota intestinal.
Pues bien, además de su papel en la terapia para diabéticos, es el único fármaco del que se sospecha que es antienvejecimiento. Todo empezó por una observación de que los diabéticos tenían mucha menos incidencia de cáncer, Parkinson y Alzheimer. Esto es, enfermedades asociadas al envejecimiento. Los diabéticos no viven más porque tienen esa enfermedad, la diabetes, pero sí se puede decir que los que tomaban la metformina estaban mejor que los que no lo hacían. A partir de ahí se hicieron estudios con animales, donde también se observó un retraso del envejecimiento al administrar metformina. Además, ya hay también estudios sobre el mecanismo por el cual logra este efecto. En 2016, por primera vez, la FDA aprobó el primer ensayo clínico para comprobar si la metformina efectivamente frena el envejecimiento o no. Actualmente hay más ensayos clínicos en marcha o preparándose, para evaluar la posible eficacia de la metformina como terapia antienvejecimiento. El más importante de ellos, TAME, es un estudio multicéntrico llevado a cabo en los Estados Unidos con más de 3.000 hombres y mujeres de entre 65 y 79 años. Es importante recordar que la metformina lleva décadas en el mercado y es un medicamento muy seguro, con muy pocos efectos secundarios.
EJERCICIO
La buena forma física y la longevidad se encuentran fuertemente asociados en humanos, de tal manera que el ejercicio regular disminuye tanto la mortalidad como la morbilidad (enfermedad). Así, todos sabemos que las personas que hacen pesas ganan fuerza y masa muscular. Lo que probablemente no sepa mucha gente es que también se producen cambios dentro de nuestras células. Así, investigadores de la Clínica Mayo estudiaron los cambios que se producían en la expresión de genes y proteínas en cuando se realizaban distintos tipos de ejercicio. Estudiaron sujetos jóvenes y mayores y tres modos de ejercicio: de alta intensidad (HIIT), de resistencia y combinado, durante un período de 12 semanas. Vieron cambios de expresión en numerosos genes, sobre todo en el grupo que realizaba ejercicios de alta intensidad. Los genes cuya expresión aumentaba con el ejercicio intenso coincidían en muchos casos con los que se desactivan con la edad.
Efectos moleculares de distintos tipos de ejercicios
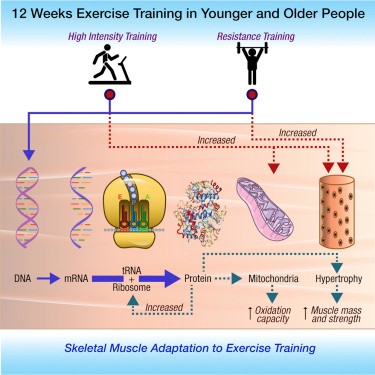
Imagen tomada de Robinson M et al., Enhanced Protein Translation Underlies Improved Metabolic and Physical Adaptations to Different Exercise Training Modes in Young and Old Humans, Cell Metabolism (2017)
Los investigadores afirman que el ejercicio «corrigió» el declive de los músculos asociado con la edad. De hecho, hay numerosos estudios independientes que, si los tomamos en conjunto, nos revelan que los efectos benéficos del ejercicio implican a las nueve características del envejecimiento de las que hablamos en el post anterior.
REPROGRAMACIONES CELULARES
La reprogramación celular es una tecnología que le valió el Premio Nobel en 2012 al japonés Yamanaka. Lo que logró es que células adultas retornaran a un estado similar al de las células embrionarias, de tal manera que a partir de ahí esas células se podían diferenciar en cualquier otro tejido. A esas células se las llama iPS (células pluripotenciales inducidas de células de tejido adulto). Podemos decir que es algo similar a devolverles la juventud a las células adultas, viajar atrás en el tiempo. Se trata de algo que es posible en los laboratorios. Se puede coger unas células, añadirles cuatro factores y las células vuelven atrás, al nacimiento. En realidad, no es que el organismo viaje atrás, sino de algo que se realiza con células de tejidos específicos. Así, por ejemplo, a un paciente con una alteración neurodegenerativa se le podrían llevar hacia atrás a algunas de sus células hasta un momento embrionario en el que las células no tienen defectos, reconstruyendo de esa manera el tejido. Suena a ficción y aún no estamos cerca de que se haga en clínica. Por ahora nos quedamos con que se hace en el laboratorio y sirve para hacer modelos de enfermedades. Aquí tenéis un artículo muy interesante sobre como se ha logrado retrasar el envejecimiento en ratones por medio de la reprogramación celular.
EDICIÓN GENÓMICA
Se trata de otra posibilidad teórica con técnicas que ya se usan en laboratorio. Sabemos ya desde hace tiempo que un cambio en una sola letra del genoma puede provocar una enfermedad. El envejecimiento surge porque vamos almacenando muchos de estos cambios a lo largo de la vida Hoy en día podemos corregir esos errores, editar el genoma con una precisión altísima, como si fuera una cirugía molecular de precisión.
About the Author: Alberto Morán
11 Comments
Leave A Comment Cancelar la respuesta
Este sitio usa Akismet para reducir el spam. Aprende cómo se procesan los datos de tus comentarios.








Estamos como siempre, se hace el gran descubrimiento y solo se hacen pruebas con ratones, porque no se prueba en humanos si es algo tan deseado y esperado por los humanos, ya podemos esperar porque todo debe de ser mentira podrida, siempre se quedan las pruebas unicamente realizadas en ratones.
La investigación sigue casi siempre unos pasos. En primer lugar se trabaja en cultivos celulares. Estos cultivos son células generalmente humanas que se mantienen en pequeñas placas en unas condiciones controladas. Ahí puedes añadir los componentes que quieras y hacer experimentos variados. Aunque sean células humana su correlación con lo que pasa en un organismo completo no es muy alta. Suele servir para ver mecanismos, estudiar como funcionan, por ejemplo, las rutas de señalización de dentro de la células, hacer pruebas con compuestos que podrían ser candidatos a fármacos, etc. Luego hay otro nivel que son los animales de experimentación. Por cuestiones éticas se intenta reducir cada vez más su empleo, pero por ahora siguen siendo irremplazables. Se utilizan distintas especies, como el gusano C. elegans, la mosca D. melanogaster, ratas, ratones, incluso simios (pero esto es menos frecuente). Aquí ya estamos trabajando con organismos completos, por lo que todo se acerca más a la realidad de lo que pasa en un cuerpo humano. Y luego viene el último nivel. Creo que no hace falta explicar que NO es ni ético ni legal hacer determinados experimentos con humanos. De hecho casi no se puede hacer ningún experimento. Para llegar a probar algún fármaco en humanos primero tiene que haber probado en animales. Solo si en todas las fases anteriores algo parece seguro y prometedor se puede iniciar una prueba muy controlada en un pequeño grupo de personas.
Y no, no es todo mentira. Si todo fuera mentira, ahora mismo no tendrías casi ninguno de los medicamentos que tantas vidas han salvado.
Muy interesante el artículo. Gracias x informar.
¡Gracias a ti! Nos alegramos de que te resulte interesante.
Saludos
Muchas gracias, Julián. Los opciones en el ámbito laboral, si vas a hacer la carrera de biotecnología son variadas, pero depende un poco del país en el que estés. Yo te cuento, lo que conozco, que es España. La primera opción es dedicarse a la investigación, típicamente en universidades o centro de investigación. Esto implica hacer la tesis para convertirse en doctor. También se podría hacer en empresas, pero hay menos opciones. Por otra parte también se puede plantear trabajar directamente en una empresa biotecnológica o en puestos relacionados con la biotecnología, aunque no sean empresas biotech propiamente dichas. Así, lo primero que tienes que ver es qué tipo de biotech te interesa. Tendrás que decidir si quieres ir por la rama sanitaria, la marina, agrícola… Hay muchas opciones. La más conocida es todo lo relacionado con la sanitaria (enfermedades y demás), pero hay campos muy interesantes de biotecnología en el mundo del vino, de los cultivos agrarios, por ejemplo. También hay un hueco importante en lo que son las aplicaciones industriales de la biotecnología: mejora de procesos industriales de casi cualquier tipo. También se emplea la biotecnología en procesos relacionados con el medioambiente, como la depuración de agua, la remedación de suelos contaminados…
Saludos
Del todo interesante el articulo, que bueno que existe gente seria en internet que publican artículos como estos.
Gracias!
Un saludo
Que se recomienda para evitar el envejecimiento en un paciente de 73 años?
Como es que la METFORMINA ayuda a evitar el envejecimiento? – La METFORMINA genera problemas al riñon?
El envejecimiento, como comentábamos en el post, no se puede evitar. Lo que se ha de buscar es que sea un envejecimiento saludable y, si acaso, retrasarlo. Los mecanismos por los que la metformina aún están en estudios, pero ya tenemos algunas pistas, como puedes ver aquí: http://www.redaccionmedica.com/secciones/medicina-interna/el-farmaco-para-la-diabetes-que-esconde-un-secreto-antienvejecimiento-6235 . Y no, en principio la metformina no afecta al riñón. Pero, como siempre, la administración de este fármaco ha de ser decidida y supervisada por un médico.
[…] el envejecimiento, explicando los cambios biológicos que se producen al envejecer y también las estrategias para frenar este proceso natural. Hoy os vamos a explicar cómo el equipo de Salvador Macip, al que ya […]
Muy interesante, he estado siguiendo los experimentos de David Sinclair y durante 7 meses tanto mi marido como yo tomamos 1 gramo de transresveratrol y 1 gramo de nicotinamida a diario. Mi marido aumento su energia y le crecio pelo nuevo. Yo no noté aumento en energia, ya soy una persona con mucha energia natural pero si observé incremento en el pelo, disminución del tiempo de cicatrización en cualquier corte o herida y una gran mejora en mis articulaciones. Algunas molestias al girar el cuello, al doblar loas rodillas, etc, desaparecieron. No obstante, en mi caso,
me aumento la cifra de colesterol LDL, Amilasa y Aspartato aminotransferasa. Paré los dos productos y tras 3 meses el colesterol y el aspartato han vuelto a sus valores normales y la amilasa ha disminuido notablemente pero todavia esta ligeramente por encima de los valores normales. Los tests de mi marido son normales. Yo creo que es debido a que yo peso 57 Kg y el 85 . Esperaré que la amilasa disminuya y luego empezaré por un solo producto pero la mitad de la dosis. Tengo 80 años y estoy en muy buen estado físico por lo que quisiera mantenerme bien los años que me queden de vida.